環境負荷の低い「グリーン水素」を作る技術とは。世界初、大阪大学などの研究

次世代エネルギーの一つである水素(H2)は、その製造過程で排出される二酸化炭素の量に応じて種類が色分けされている。最も排出量の少ないものを「グリーン水素」と呼ぶが、大阪大学などの研究グループが「グリーン水素」製造に関する世界初の技術を開発した。
「グリーン水素」とは
二酸化炭素は温室効果ガスとして地球温暖化の原因物質の一つとされ、世界的にカーボンニュートラル(二酸化炭素排出量実質ゼロ)が温暖化対策の重要な施策になっている。そのため、化石燃料に代わるエネルギーが求められているが、水素もその一つだ。
水素は地球上で最もたくさんある元素であり、燃やしても二酸化炭素を出さないクリーンエネルギーであること、化学工業におけるアンモニアやメタノール生産などの還元剤や反応ガスとして、また半導体製造での雰囲気ガスとして、あるいは鉄鋼業で二酸化炭素排出を減らすため、水素を使った製鋼技術が注目されるなど、燃料電池などの次世代エネルギーのみならず多種多様な産業で活用されている。
だが現在、水素の主な製造方法は化石燃料のメタンを水蒸気と反応させて水素と炭酸ガスを作る方法(水蒸気改質)によるものであり、その製造過程で多量の二酸化炭素や一酸化炭素が排出される。また、この方法はコストが低いものの、高温の反応温度が必要なために多くのエネルギーが必要だったり、触媒にニッケルやロジウムなどを使ったりするため、むしろ環境負荷が高くなる。
その他、バイオマスを利用したり、製鉄業などの別産業から副次的に水素を製造するなどの方法もあるが、いずれもコスト高だったり工程が煩雑だったりして現実的ではない。
こうしたことから水素製造は、二酸化炭素の排出量によって化石燃料からのものを「グレー水素」、化石燃料からでも二酸化炭素を回収・貯蔵するものを「ブルー水素」などと色分けし、現状では95%以上の水素がグレー水素から製造されていると考えられている。
これは電気自動車でも同様だが、クリーンエネルギーである水素がその製造過程で多量の二酸化炭素を排出してしまうという皮肉なことになっており、再生可能エネルギーや水から水素を安価に作り出す「グリーン水素」の製造技術が待望されている。
さらに、日本の水素の供給は多くを輸入(オーストラリアやブルネイなど)に頼っており、世界各国が水素を求めることで供給不足になり、資源安全保障の観点からの危険性もある。
水電解による水素製造
水(H2O)は、酸素と水素の化合物だ。水を電気エネルギーによる化学反応で分解し、水素を製造することが可能だが、これを水電解(吸熱反応)といい、水の還元(水素発生反応)と水の酸化(酸素発生反応)の反応が起きて水素を得られる。
つまり、水から水素を得るためには、どうしても酸素ができてしまう。逆にいえば、酸素の発生反応の高効率化が水電解による水素製造のキモともいえる。
また一般的に、水電解による水素製造は、分離操作がなく、可動部が少なく、設備容量に応じて小型化や大型化が簡単にでき、太陽光発電や風力発電などの再生可能エネルギーを電力や熱源として使えばコストも安い方法とされる。
水電解に必要なのは、電解質、電極、隔膜(電解質膜)であり、水電解技術にはアルカリ水電解、固体高分子形水電解、高温水電解などがある。電解質には水酸化カリウム(KOH)、フッ素系カチオン交換膜などが、高活性電極材料(酸化反応側のアソード、還元反応側のカソード)にはニッケル、鉄、酸化イリジウム、酸化ルテニウムなどが使われ、一般的にアルカリ水電解は低コストだが低効率で大型、固体高分子形水電解は高効率だが高コストで小型とされる。
これまで水電解による水素製造の研究開発では、主に電極の材料の検討が進められ、高効率で低コストな材料と安定性と信頼性の高い方法を模索してきた(※1)。そのため、安定性が高く最適な電極の開発に注力され、ニッケル鉄合金や酸化イリジウムなど多くの電極用の材料が開発されている。
世界初の新たなブレークスルー
電極材料の探索や開発により、水電解による効率は向上してきたが、さらなる高効率のためには電極材料に加え、新たなブレークスルーが必要と考えられている。そのため、大阪大学などの研究グループ(※2)は、アルカリ水電解による水素製造で効率が低下する原因とそのメカニズムを世界で初めて解明し、米国の化学雑誌に発表した(※3)。
同研究グループは、アルカリ水電解による水の酸化(酸素発生反応)の反応速度の低下要因が、電解液(水分子)のpH(水素イオン濃度指数、H+の量)による影響にあるとし、電解液のpHの違いによって、反応中間体(反応の途中段階で生じる化学種)と電極と極めて近い位置にある電解液との相互作用、電解液によって媒介された反応中間体同士に働く相互作用などが変化し、電極表面上の反応中間体に影響をおよぼすことを明らかにした。
前述したように、酸素の発生反応の速度が遅いと水電解による水素製造の高効率化ができない。酸素発生反応が、水素発生反応の足を引っ張るからだ。
水電解などの電気化学反応では、途中段階で反応中間体が生じる。この反応中間体の安定性が、その電気化学反応の速度を決め、反応中間体の安定性は、電極表面に吸着した(電極と結合)状態で存在するため、電極の特性によって大きく左右される。
これらの結果から同研究グループは、電解質のpH、反応中間体との相互作用などから電解液の効果を組み込んだ新たな提案(火山型プロット)をした。
火山型プロットとは電極触媒の設計図のようなもので、これまでのアルカリ水電解による水素製造では反応中間体と電極の相互作用だけのプロットだったが、同研究グループはそこに世界で初めて電解液の項目を加えたということになる。
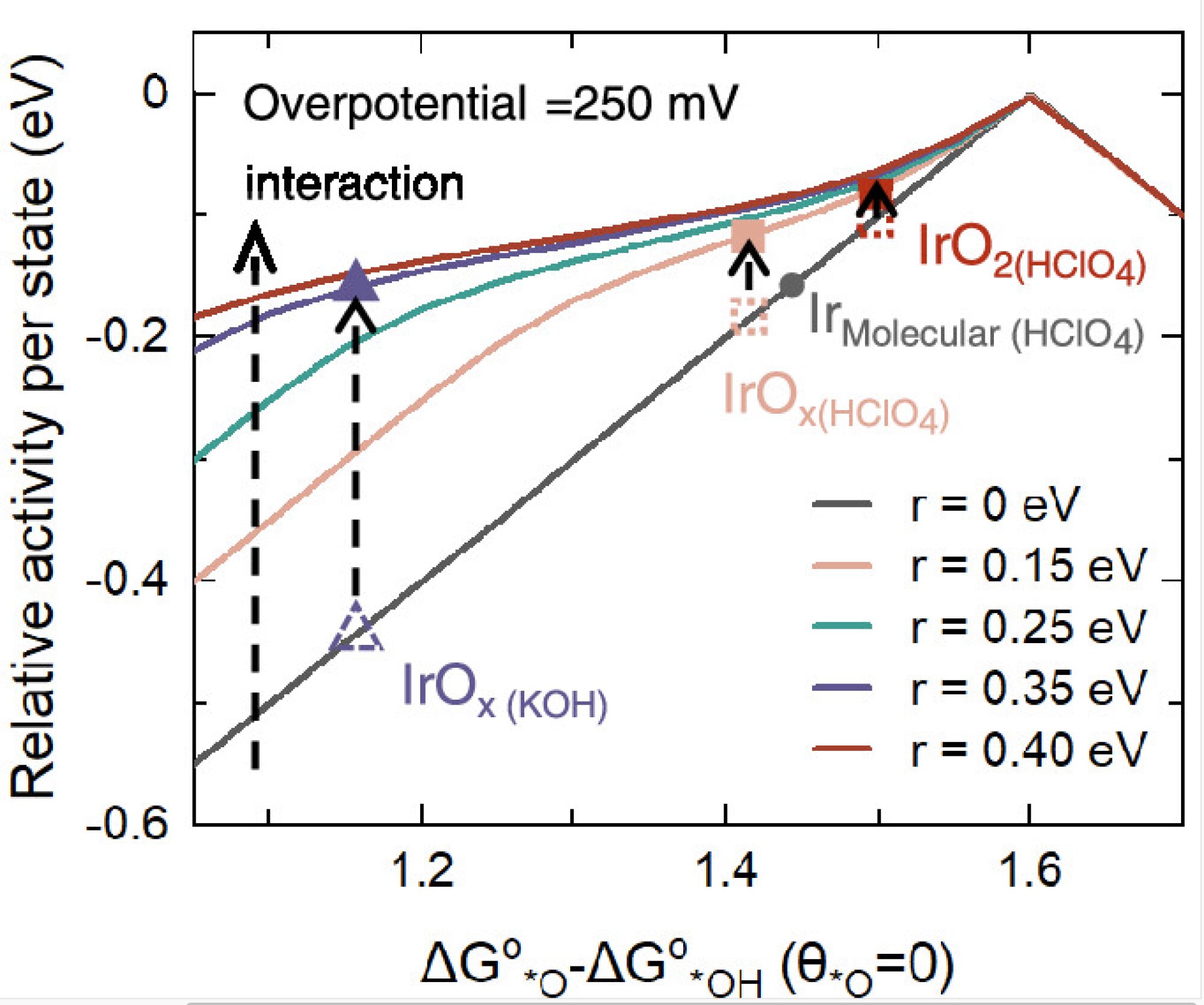
上のグラフは大阪大学のリリースから引用したものだが、黒い実線(従来の反応中間体と電極)より、同研究グループによる電解液の効果を反映させた設計案のほうが活性(縦軸)を上げ、電極由来の特性(横軸)を変えることなく酸素の反応速度を向上させられることがわかる。
これまでほとんど考慮されてこなかった電解液を新たに設計し直すことで、従来の電極材料の改良と組み合わせ、酸素の反応速度の遅さによって高効率化が阻害されている水電解による水素製造のイノベーションにつながる。再生可能エネルギーを利用した「グリーン水素」の製造に、大きな影響をおよぼす研究成果といえる。
※1:光島重徳、藤田礁、「水電解による水素製造の現状と展望」、Electrochemistry, Vol.85, Issue1, 28-33, 27, December, 2016
※2:大阪大学 産業科学研究所 片山祐准教授らの研究グループ、英国インペリアルカレッジロンドンの研究グループ
※3:Caiwu Liang, et al., "Role of Electrolyte pH on Water Oxidation for Iridium Oxides" Journal of the American Chemical Society, Vol.146, Issue13, 8928-8938, 25, March, 2024










