脳へ薬剤を送りこめ〜「脳関門」をどう突破するか

脳には異物を排除するバリア機構があり、薬を脳へ運び入れることがこれまで難しかった。今回、東京医科歯科大学などの研究グループが認知症などの神経難病の治療に応用できる薬を脳の中へ送り込む新技術を開発した。
身体にある関門とは
脳には血液脳関門(Blood-Brain Barrier、BBB)や血液脳脊髄液関門(Blood-Cerebrospinal Fluid Barrier、BCSFB)があり、網膜には血液網膜関門(Blood-Retinal Barrier、BRB)があり、これらが脳や網膜へ必要な物質以外の異物が簡単に入らないようにしている。そのため、薬を患部へなかなか到達させられず、アルツハイマー病などの脳神経疾患や糖尿病性網膜症などの網膜の病気の治療は難しいとされてきた。
こうした関門は生体が備えたバリア機構で、身体のあちこちへ酸素やグルコースやアミノ酸などの栄養などを運ぶための血液が通る血管にある。脳の毛細血管も必要な物質を通すが、血管の細胞が密着している隙間よりも大きな分子の物質は通さない。
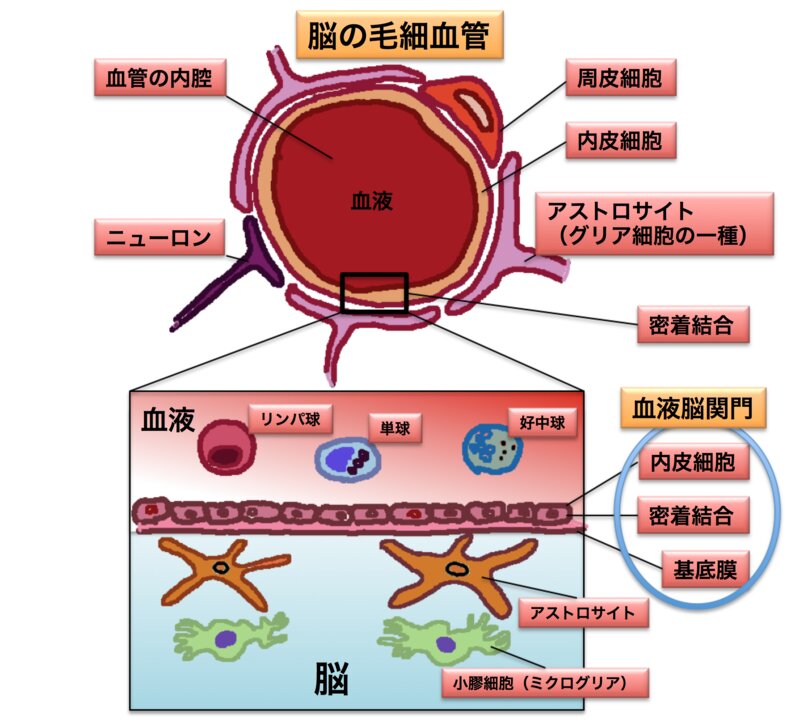
脳内の毛細血管と血液脳関門の図。周皮細胞というのは血管の成熟や安定化、血液脳関門の維持、虚血時の神経保護修復などを担っていると考えられる細胞。Timothy M. Cox, "Expert Reviews in Molecular Medicine." Cambridge University Press, 2003を参考にして筆者が作画
ところが、酒を飲むとアルコール(エタノール)が消化器官を経て肝臓から身体の中に吸収されるが、アルコールは分子量が小さく水溶性でも脂溶性でもあるので、脂溶性の物質を透過させやすい血液脳関門から脳へ入ってしまう。そのため、脳の機能へ影響を与え、酔っ払ってしまうというわけだ。
また、タバコを吸うとニコチンが肺から吸収され、血液から素早く脳へ到達し、ニコチン性アセチルコリン受容体という脳内の報酬系を刺激する。だが、ニコチンがどうやって血液脳関門を通ることができるのか、そのメカニズムはよくわかっていない。おそらくニコチンの持つイオンの性質(カチオン、陽イオン)が作用しているのではないかと考えられている(※1)。
最近の研究では、妊娠中の母子の間にある胎盤にも関門があることがわかってきたが、母体由来の腸内細菌などの微生物が血液脳関門の形成に影響を与えているのではないかという研究もある(※2)。共生菌が脳の機能をつかさどっているということかもしれず、減菌や殺菌が必ずしもすべていいわけではないことを示唆する。
脳のバリアをどう突破するか
このように脳関門や網膜関門などの身体の関門は、外部からの異物の侵入を防ぐバリアでもあるが、同時に患部へ薬を運び入れるのを阻害する厄介な機構だ。血液脳関門からはいくら薬を入れようとしても目的の0.1%ほどしか到達できないという状況が続き、なんとかして血液脳関門を突破しようと世界中の研究者が試みてきた。
血液脳関門などは日本の研究が先端をいっているようなところもある。これまで小膠細胞(ミクログリア、Microglia)を使った名古屋大学の研究グループの研究があり(※3)、最近では日本の研究グループによる脳内へ薬剤を運ぶナノマシンを開発したという発表もあった(※4)。これは東京大学などの研究グループが開発したグルコース濃度の変化という外部刺激に応答して血液脳関門を高効率で通過する直径30nmの微小高分子で、水溶液の中で自己組織化するナノマシンだ。
こうした血液脳関門への挑戦として最近、新たな研究成果が発表された。日本の東京医科歯科大学の研究グループによるものだ(※5)。がんやアルツハイマー病など遺伝子変異が疑われる病気に対し、そのターゲットとなる遺伝子の機能を失わせたり減退させたりする作用(アンチセンス)を持つ薬を使う。あるタンパク質によって血液脳関門を通過させ、脳の中枢神経系へ薬を到達させることができたという。
アンチセンスの核酸医薬で用いられる薬(相補的なmRNA)は分子標的薬などといわれ、周囲の無関係な遺伝子にほとんど影響を及ぼさず、ターゲット遺伝子にだけ作用させ、病気やその進行を抑えることが可能と考えられている。だが、アンチセンス核酸薬が血液脳関門を通過できる量はあまりにも少なく、これまで患部の遺伝子に作用させることが難しかった。
東京医科歯科大学のリリースによれば、脳内の毛細血管の細胞が接する部分の密着結合(血液脳関門)に作用するアンギュビンディン1というタンパク質の断片をマウスに静脈注射し、その後、アンチセンス核酸薬を静脈注射したところ、アンチセンス核酸薬が従来より大量に脳や脊髄に到達し、ターゲットとなる遺伝子の発現が約40%抑制されたという。
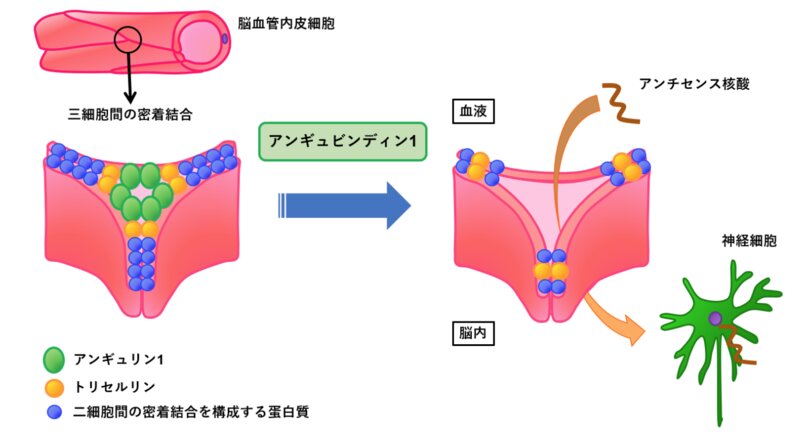
血液脳関門がある血管の3つの細胞の結合を制御するアンギュビンディン1というタンパク質断片により、血液脳関門に隙間を空けてアンチセンス核酸薬が脳内へ送り込む。Via:東京医科歯科大学のリリース
現段階ではマウスでの実験だが、研究グループは血液脳関門がある血管の3つの細胞の結合を制御するという薬物送達の手法の成功は世界初という。将来的には、アルツハイマー病を含めた認知症や脊髄性筋萎縮症などの神経関連の難病の根本治療も可能となるかもしれない。
※1-1:Yuma Tega, et al., "Functional expression of nicotine influx transporter in A549 human alveolar epithelial cells." Drug Metabolism and Pharmacokinetics, Vol.31, Issue1, 99-101, 2016
※1-2:Shin-ichi Akanuma, et al., "Role of cationic drug-sensitive transport systems at the blood-cerebrospinal fluid barrier in para-tyramine elimination from rat brain." BMC, Fluids and Barriers of the CNS, Vol.15:1, 2017
※2:Viorica Braniste, et al., "The gut microbiota influences blood-brain barrier permeability in mice." Science Translational Medicine, Vol.6,(263), 263ra158. doi:10.1126/scitranslmed.3009759, 2014
※3:Fumihiro Imai, et al., "Neuroprotective effect of exogenous microglia in global brain ischemia." Journal of Cerebral Blood Flow & Metabolism, Vol.27, 488-500, 2007
※4:Yasutaka Anraku, et al., "Glycaemic control boosts glucosylated nanocarrier crossing the BBB into the brain." nature COMMUNICATIONS, DOI: 10.1038/s41467-017-00952-3, 2017
※5:Satoshi Zeniya, et al., "Angubindin-1 opens the blood-brain barrier in vivo for delivery of antisense oligonucleotide to the central nervous system." Journal of Controlled Release, Vol.283, 126-134, 2018