高額がん治療薬「オプジーボ」が半額に 薬価はどう決まる?
研究開発に15年、当初は類似薬もなく
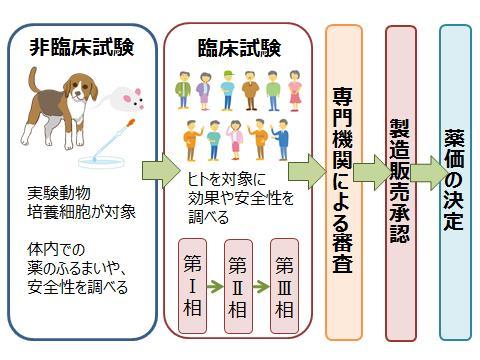
新しい薬が私たちのもとに届くまでには、長い道のりがあります。実験動物や実験室で育てている細胞を使った非臨床試験、健康な人や患者さんを対象にした3段階の臨床試験で効果や安全性を何年もかけて確認し、専門機関による審査を受けなければなりません。 それに合格してようやく、日本での製造・販売が許可されます。一般的に、非臨床試験から承認・発売までにかかる期間は、9~17年。研究を始めた化合物が薬として世に出られる確率は、2万分の1とも言われています。 薬価が決まるのは、その最後の段階です。
薬価は、厚生労働省の中央社会保健医療協議会(中医協)が、一般にも公開されている基準(「薬価算定基準」という)に沿って決めています。中医協は、健康保険に関わる人々(保険料や診療報酬を支払う側)、医療関係者(診療側)、その分野に詳しい「有識者や学識経験者」などと言われる方々(公益側)からなる組織です。 オプジーボの薬価はどんな根拠で決まったのでしょう。オプジーボが承認されたとき、似たような仕組みでがんに効く薬(類似薬)はありませんでした。このような場合、薬価は「原価計算方式」という方法で決められます。これは、実費をもとに計算した原材料費に、いろいろな調査・統計から計算できるその他の費用を足し算する方法です。
オプジーボの場合、遺伝子組換えをした細胞が作り出すタンパク質が有効成分となっています。培養皿の中の細胞自体が「工場」となり 、できあがった有効成分を取り出して薬にしているのです。原料の化学物質を大きな工場のラインであれこれして作るのとはだいぶ異なります。そのため、製品をつくるためにかかる費用は、一般的な薬に比べかなり高額になります。 また、注目したいのは研究開発費。オプジーボの開発には15年という長い年月がかかっており、具体的な金額は公表されていませんが、少なくとも1,000億円以上の費用がかかっていると考えられます。しかし、承認当時、オプジーボによる治療の対象になったのは、「悪性黒色腫(メラノーマ)」という、患者さんの数が少ない、珍しい皮膚がんの一種だけでした。つまり、お金をかけてつくったのに少ししか売れない。それだと製薬会社は困ってしまうし、あえて患者さんの少ない難病の薬を開発する意欲が失われてしまいます。そのため、オプジーボの薬価には研究開発費と、その革新性や治療における意義(悪性黒色腫に使える薬は非常に限られている)を考慮した利益も多めに含まれています。 さらに、オプジーボは世界で最初に日本で承認されたため、他の国と薬価値段を比較し、調整することができませんでした。もし他の国の薬価を参考にできていれば、もう少し安くなっていたかもしれません。実際、日本でのオプジーボの薬価値段は100mgで約73万円ですが、アメリカでは約30万円、イギリスでは約14万円です。 ちなみに、つい最近、「キイトルーダ」というオプジーボと全く同じ仕組みでがんと闘う薬が日本でも承認されました。この場合は、すでに類似薬(オプジーボ)が存在するので、「類似薬効比較方式」という、先ほどとは別の方法で値段が決まります。オプジーボの薬価を基準にして、キイトルーダの方が薬として優れているところがあれば値段を上乗せしていく方式です。海外の薬価も参考にしつつ、日本での薬価も近いうちに決まるものと思われます。