信頼を得るには、知ってもらうことから。新型コロナワクチン承認の議論を公開する米国
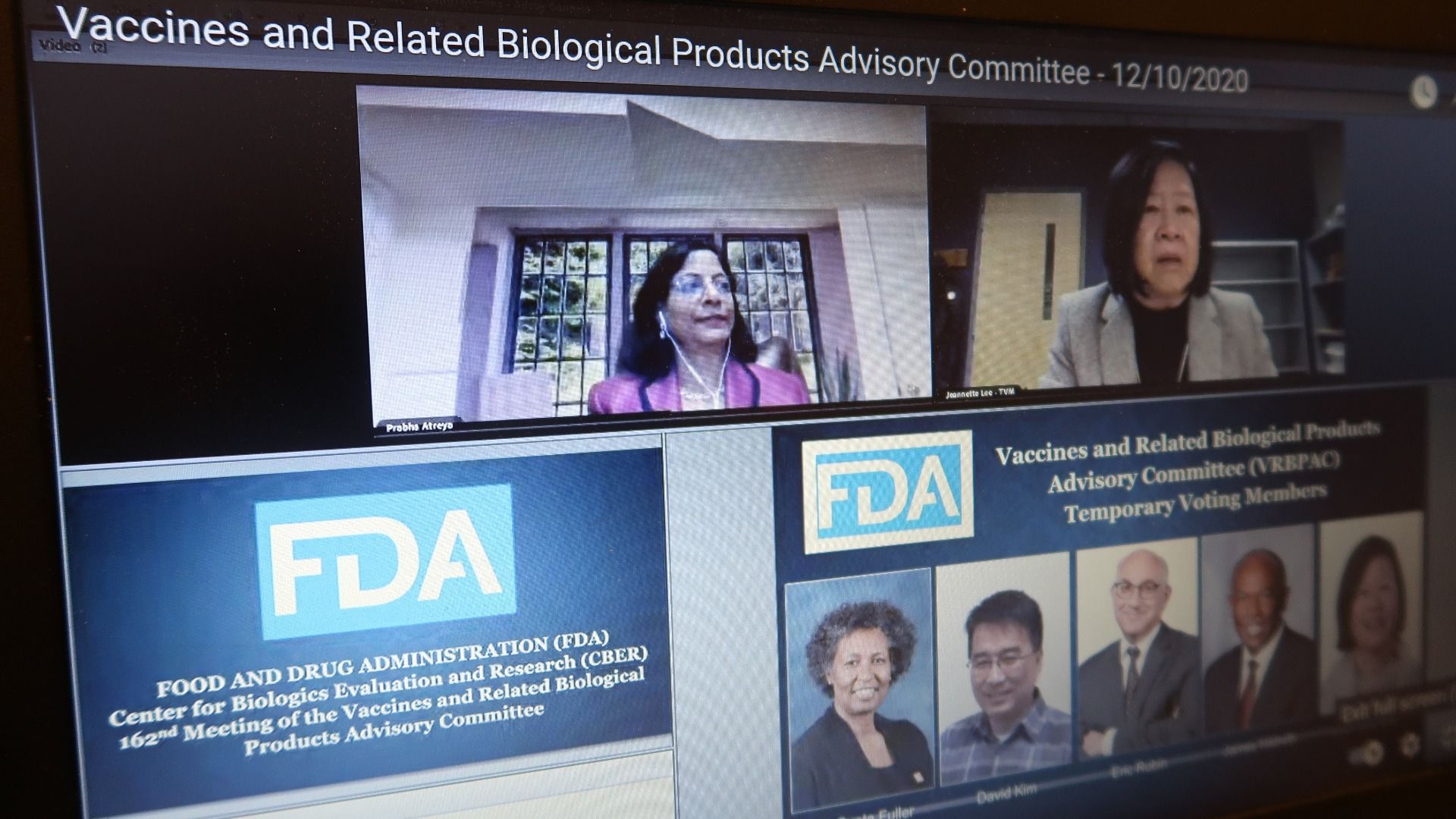
すべて見せます、米国のワクチン承認審議
日本では2月12日に薬事・食品衛生審議会を開き、米ファイザー社と独ビオンテック社が共同開発した新型コロナワクチン「コミナティ筋注(製品名)」の承認可否を審議する。認められれば、厚生労働省が2月14日にも正式承認した後、医療者を対象に接種がはじまるようだ。米国でも最初に使用承認審査の対象となったのはファイザー社のワクチンで、昨年12月10日に米食品医薬品局(FDA)のワクチン・関連生物製剤諮問委員会(VRBPAC)が、承認に関わる審議を行った。
コロナ禍であり、日本も米国もウェブ会議。ただし大きく違うのは、日本は午後6時から午後8時までの2時間の予定で、「企業の知的財産等が開示され、特定の者に不当な利益もしくは不利益を与えるおそれがある」という理由で非公開(注1)。
一方、米国では「これまでにない短期間で開発された新たなワクチンへの信頼感を高めるためには、承認過程も透明性を高める」という理由で、午前9時から午後6時まで、短い休憩をはさみながらの8時間以上にわたる当日の審議すべてをライブ動画で配信している点だ(注2)。また審議で使われるプレゼン資料も、審議の2日前までには公開されている(注3)。
臨床試験の結果を見るだけじゃない
政府の諮問委員会というと、専門的な学者の集まりをイメージしがちだが、実際には、感染症専門医や、小児科の感染症医、公衆衛生の疫学、病理の研究者など第一線の現場で新型コロナと対峙している23人。うち女性は8人で、人種的にも多様な構成だ。
審議会では、まずFDAが緊急使用許可に関する判断基準について説明。緊急使用許可は、死をもたらす深刻な疾病について、他に予防法や治療法が存在しない際に、臨床試験データをもとに使用申請が行われた薬剤について、その時点で判明している利益が、不利益またはリスクを上回っていれば許可の判断となる。
米疾病対策センター(CDC)からは最新の新型コロナウイルスの状況(疫学)や、緊急使用許可や承認が出された後のワクチンの安全性や効果のモニタリング方法、ワクチンの配布計画に関する説明もあった。また臨床試験でプラセボ接種を受けた人は、いつの時点で本物のワクチンを接種すべきかという問題もあった。臨床試験の結果に基づき、緊急許可を出せば終わりではなく、むしろそこからが大変な仕事になるのだと感じた。
市民団体も積極的にモノ申す
短い昼食休憩の後は、パブリック・ヒアリング。一般市民は事前に意見を提出することができ、審議で正式にプレゼンテーションをする機会もある。時間が限られているため、プレゼン希望者が多いと抽選になるそうだが、この日は一人あたり3分間で、患者の権利擁護、医薬品の安全監視、消費者団体、医療研究グループ、人権団体の代表ら20人が参加した。
正式プレゼンをした人は、やはり医療の専門知識を持つ人が多かったが、迅速な安全情報の収集やマイノリティへのワクチン配布、妊婦、HIV感染者、がん患者などへのワクチン接種の安全性情報の必要性、正確なワクチン情報の重要性など、様々な指摘を行った。またファイザーの初期臨床試験参加者が、自らの参加経験とワクチンの必要性について述べる場面もあった。
その後、ファイザー社のワクチン開発部門の副社長らがmRNAワクチンの作用機序、臨床試験の実施内容と結果を説明。諮問委員との質疑応答では、ビオンテック社CEOのウグル・サヒン博士が質問に答える場面も。国境を越えて当事者が討議に参加できるのは、ビデオ会議の強みだろう。最後に臨床試験結果について、FDAとしてのデータ分析結果に関する説明が行われた。
熱意と責任が見える審議会
一般の人がこうした審議を聞いてわかるのか?と思うかもしれないが、委員の医師らは技術的なことよりも、一般の人が安全に使えて、本当に役に立つワクチンなのかという観点で質問するので、案外とわかりやすい。例えば16歳以上を接種対象としているが、この臨床試験では16歳、17歳を後から試験対象に加えたため、参加者が少ない。少ないデータをもとに16歳以上はOKと判断してよいのか。妊婦や15歳以下の子供は試験対象に含まれていないが、こうした対象者のために今後どのように安全性と有効性を調べていくのかなど、私たちが知りたい内容も多い。
時に「聞こえますか?」、「消音になっていますよ」、「回線が不具合です」など、ビデオ会議ではお決まりのもどかしさを強いられながらも、可能な限り良い判断を下せるよう、長時間にわたり様々な質疑応答を繰り返す委員の真摯な様子に、誠実さが見てとれる。そして最後は、その時点で分かっている事実をもとに、このワクチンは利益がリスクを上回るか?という質問に対して、各委員が自らの責任と判断でYESかNOで投票するところまで、すべてライブ動画で公開しているのだ。
継続的な安全性監視と情報公開
緊急使用許可審議の時点では、ワクチン接種後の長期的な副反応はわからないが、臨床試験では接種後2年までフォローアップを続ける。またCDCでは新型コロナワクチンの接種を受けた人が、スマートフォンを使って副反応を報告できる「v-safe」システムを開発。登録すると、接種後1週間は、毎日、体調を尋ねる質問メッセージがスマホに送られてくる。懸念を呼ぶ副反応報告があれば、CDCが直接、あるいは接種医療機関を通して本人への連絡を含めたフォローを行う(注4)。
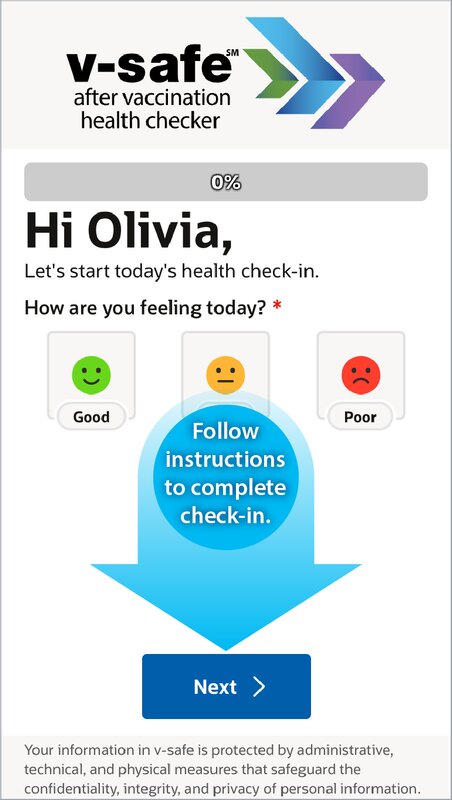
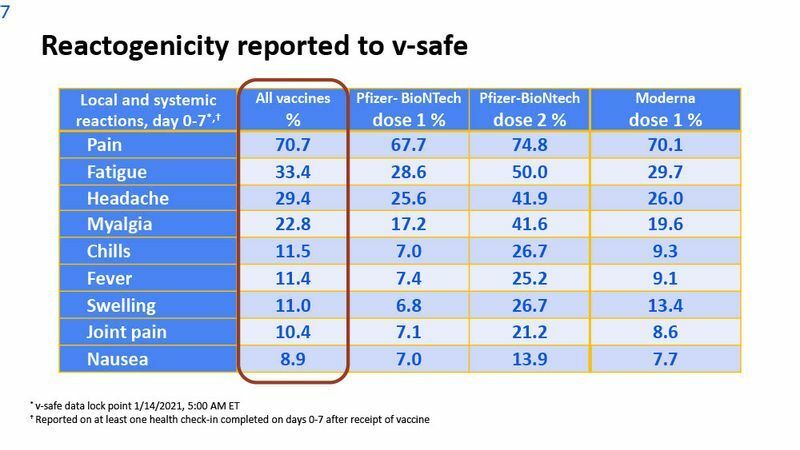
その後は週1回のペースで、5週間にわたり、体調確認のメッセージが送信される。一方、ワクチン接種機関やファイザー側は、CDCやFDAに対して定期的に副反応を報告する義務がある。こうした様々なネットワークを使って、継続的にワクチンの安全性をワクチンに関する諮問機関(ACIP)で監視していくのだ。1月27日に行われたACIPでは、1月14日までにv-safeシステムで接種者から報告された副反応のまとめも公開している。(注5)
米国の場合は、公開される情報があまりに多すぎて、そんなに見ている暇はないというのが市民の本音だろう。それでも、例えばFDAが公開したファイザーのワクチン緊急使用許可にかかわる8時間以上のマラソン審議動画はこれまでに30万回以上、ケーブルテレビ局のCNBCによる同ライブ動画配信は49.5万回以上、PBS(公共放送)では4.5万回以上視聴されている。
新しいワクチンに対して不安を抱くのも、様々な情報を求めるのも当然のこと。忙しいなら、各種メディアの報道や、コロナ対策本部の公衆衛生当局者らへのインタビューでキーポイントだけ知ることができるのだが、残念ながら「メディアは信用できない」という人も多いようだ。
市民がツイッターやフェイスブックで目にする怪しいワクチン情報を信じてしまうと嘆く前に、市民の「何を信じて良いかわからなくて不安」、「もっと知りたい」に応えるために、政府はできる限り多くの正確な情報を公開し、市民の信頼を得られるよう全力をあげるしかない。
関連リンク
注1:薬事・食品衛生審議会 医薬品第二部会を開催します (mhlw.go.jp)
注2:2020年12月10日にファイザー/ビオンテック開発のワクチン緊急使用許可を審議したワクチン・関連生物製剤諮問委員会(約8時間40分のビデオ、英語)
注3:12月10日のワクチン・関連生物製剤諮問委員会の審議で使われた資料も、パブリック・コメント参加の方法も、審議のビデオもすべて公開。(FDAサイトのページ、英語)
注5:1月27日のACIP会議の資料もすべてCDCのサイトで公開 (英語)。記事中の画像で使った副反応のデータは、Dr.T ShimabukuroのCOVID-19 Vaccine Safety Updateから。(英語)