体脂肪を落とす?コレステロールを下げる?ウワサの「機能性表示食品」とは

「体脂肪とBMIを落とす」
「悪玉(LDL)コレステロールを下げる」
最近、こんな表示とともに「機能性表示食品」と書かれた食品・サプリメントなどを、コンビニやスーパーで目にする機会が増えたと思いませんか?
消費者庁のデータベースを調べてみると、900件以上がヒットします。(届け出が撤回されたものも含まれるようです)。この制度、始まってわずか2年ですが、かなりのスピードで種類が増えているようです。
ある食品をとるだけで、体脂肪が落ちたりコレステロールが下がったりするとしたら嬉しいことですが、安全性や効果はどうやって確かめられているのでしょうか?そもそも「機能性表示食品」って、どんなもの?調べてみました。
「機能性表示食品」とは
機能性表示食品は、国(消費者庁)が2015年に始めた制度です。
消費者庁のパンフレットには次のような説明があります。
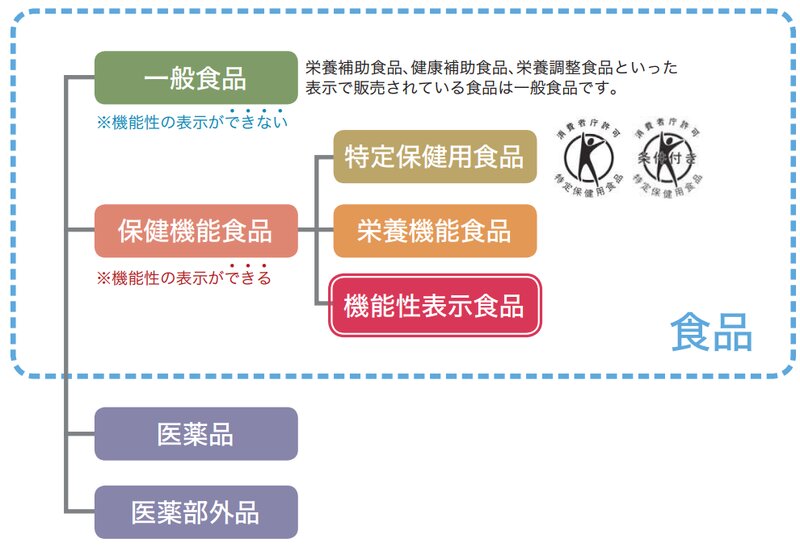
ある食品に、例えば「体脂肪の増加を抑える」というような機能性(作用)があると言われると、消費者としてはそれを選びたくなりますよね。でも一般の健康食品の場合、そのような宣伝文句を表示することはできません。
内容に誇張があったり、根拠が無かったりした場合、購入した消費者が損をしてしまいますし、食品とはいえ通常の生活でとらないようなものを大量に摂取すると、どんな影響があるかわからないからです。
ただ例外もあります。例えば特定保健用食品(「トクホ」という名前でおなじみ)は、消費者庁が企業から安全性や機能性を証明するデータの提供を受け、個別に審査したうえで「こんな表現なら表示して良いよ」と許可しています。
ただトクホには、申請に必要なデータを得るための試験に多額のお金が必要だったり、審査に長い期間がかかったりする傾向がありました。大企業はそれでも良いかもしれないけれど、資金や体力のない中小企業は申請が難しくなるかもしれません。消費者の立場としても、もし良い商品があるとしたら、その情報を知れないのは残念な気もします。
そこで2年前、「機能性表示食品」という新しいカテゴリーが作られました。
トクホのような「国による審査」を行わず、安全性や機能性について企業の責任で調べて届け出るだけで良いよ!としたのです。企業にとって、より手軽に製品のメリットをアピールできるチャンスが生まれたことになります。制度開始から2年もたたず、500件を超える食品が届け出されました。
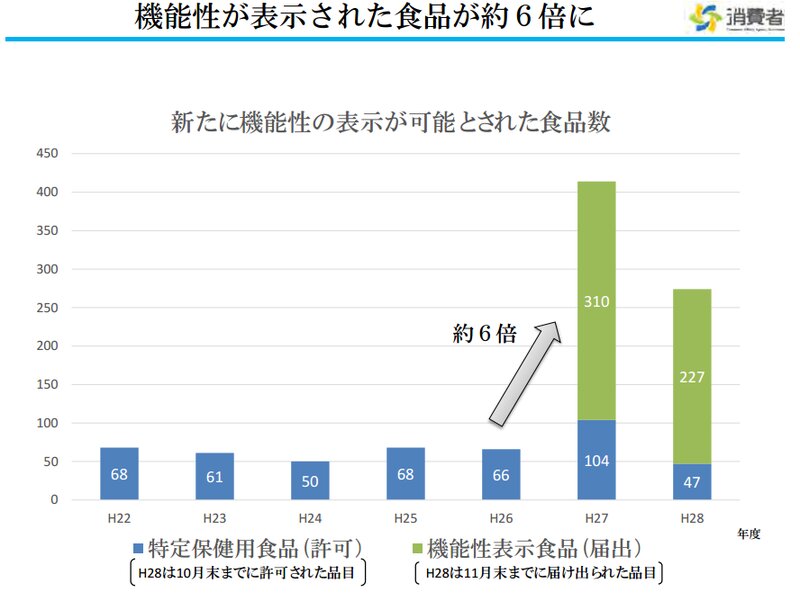
でも「審査なしでOK」にしちゃって、本当に大丈夫?という気もしますよね。とはいえ、そもそも多くの人が口にする製品を作っている企業ですから責任感は強いでしょうし、届け出た内容は消費者庁のサイトで公開されるので、変なデータを提出したら問題になるかもしれません。信頼してもよさそうな気もしますよね。
機能性の科学的根拠 結論の76%に「不備」
ところが去年、企業が届け出た資料を調べたところ、その多くに不備が見つかった、とする報告書が公開されました。
「機能性表示食品」制度における機能性に関する科学的根拠の検証-届け出られた研究レビューの質に関する検証事業
どういうことでしょうか。少しだけ専門的な話になりますが、できるだけ分かりやすくお伝えします。
機能性表示制度では、企業が自分の製品の機能性を示す方法として研究レビュー(システマティックレビュー)というものを認めています。

肯定的な結果だけでなく、否定的な結果もすべてあわせて、「機能性がある」と認められるかどうかを総合的に判断するものです。
例えば「体脂肪を減らす」ことが期待される成分を含む食品があるとして、それを証明しようとした場合のことを考えます。
まず考えられるのは、実際にその食品をたくさんの人に長い期間食べてもらい、食べなかった人と比較する試験をすることです。食べた人だけ体脂肪が減っていれば、機能性がある可能性が高いといえそうですよね。ただ試験には、お金と時間と手間がかかります。
ここで仮に、その成分はとても有名なもので、過去に国内外で様々な研究が行われていたとします。
そうした研究をたくさん集めて評価したところ、「機能性がある」と結論した研究も「ない」と結論した研究もあったのですが、どうやらたくさんの人を調査した「質の高い研究」に限ってみると、「機能性がある」としたものが多くなりました。であれば、わざわざ改めて試験を行わなくても、「この成分には機能性がある」と言ってよさそうです。
このように、『過去のたくさんの研究を決められた方法で評価し、結論を導く』のが研究レビュー(システマティックレビュー)の考え方です。
適切に行われるのであれば、むしろ「この食品を売りたい!」と考える企業自身が試験するより信頼性が高い結論が得られそうな気もします。さらに企業側から見ると、試験にかかるお金と手間と時間を省略できるメリットがあります。
実際、機能性食品を販売している企業の多くが研究レビューを採用しています。消費者庁のデータベースに登録のある907件のうち、9割以上に当たる856件が「研究レビュー」を根拠としているようです。(2017年5月12日時点)
ところが消費者庁が、企業による研究レビューを調べたところ、その多くに、方法や内容の不備があったことがわかりました。
例えば、研究レビューでは「過去の文献をどんな方法で検索するか、そして見つかった研究を、どんな基準で評価するか」など研究計画(プロトコール)を事前に決め、公開することが重視されます。そうしないと、都合の良い論文だけが見つかるように検索を操作したり、悪い結果が出た研究を排除したりする疑念がぬぐえないからです。
しかし実際のところ、企業が届け出た研究レビューのうち96.1%は研究計画を事前に登録・公開しておらず、詳細を知ることができない状態でした。
また、もっとも重要な「結論」の部分においても、バイアス(偏り)の影響を踏まえて検討したか不明瞭など76.5%に不備があったとしています。それを踏まえて、報告書は次のように指摘しています。
少なくとも、定性的な届出SR で断言的に有効性を示すことができるかどうかは大いに疑問であり、より適正な書き方が必要である。このことは、表示しようとする内容(文言)にも直結するであろう。
出典:「機能性表示食品」制度における機能性に関する科学的根拠の 検証-届け出られた研究レビューの質に関する検証事業 報告書
いま販売されている機能性表示食品には、例えば「体脂肪を落とす」など断定的な内容(文言)を表示しているものが少なくありません。報告書を読んだ印象では、それを額面通り信じて本当に良いのか?少し不安になってしまいました。
機能性表示食品 「安全性」は大丈夫?
さらに消費者庁が行った別の調査では、安全性にも不安を覚える状況が見えてきています。
・機能性関与成分の含有量が、表示値を下回っている、若しくは過剰に含まれている
・同一製品にもかかわらず2ロット(又は2パッケージ)間でのばらつきが大きい
など、品質管理上の問題点が見つかった。
消費者庁が店頭で売られている「機能性表示食品」を購入し、その成分を調べる抜き打ち検査を行ったところ、成分が表示値を下回っていたり、過剰に含まれているものなど、品質管理上の問題がある製品が見つかりました。
通常の量なら問題がない食品であっても、成分が過剰に含まれていたときに、本来とは異なる作用を体に及ぼさないのか?ちょっと心配になってきます。
機能性食品の安全性については、最近、別の報告も出てきています。
4月10日、東京都消費生活総合センターは『「危害」の消費生活相談の概要』を公表しました。
そのなかで「とくに重篤な危害が生じた相談事例」として、40歳代の男性のケースが紹介されました。(太字は筆者によるものです)
4ヵ月程前、友人から「目のピント調節の機能性表示食品60粒入り1袋」をプレゼントとしてもらった。2ヵ月前より、製品表示どおりに1日2粒を朝と晩に分けて食用し続けた。(中略)全身のだるさとめまいが取れず、5日後にB内科医院で血液検査を受けると、翌日、B医院長より「肝臓検査値が異常に高いのですぐ来院するように」と言われた。(中略)E病院で検査を受け、危険値のため緊急入院した。担当医の所見は「当該機能性表示食品による薬物性肝炎」で、肝疾患の症状である「黄疸・全身のかゆみ・倦怠感の改善と薬害の除去治療」後、2週間前に退院した。
上記は相談者側による、いわば一方的な視点によるものです。この事例が真実か、食品が本当に原因なのかなどは確認されていません。しかし薬物性肝炎は、場合によっては死にいたることもある病気です。仮に機能性表示食品が関係があったとすれば大きな問題です。
この件について消費者庁に把握しているか、調査を行っているかなどを問い合わせたところ、「個別のケースに関する質問にはお答えを差し控えさせていただきたい」という回答でした。
機能性表示食品 どう付き合うべきか
「体脂肪を落とす」などの魅力的な言葉が大きくプリントされ、普通の食品より良質なイメージもある機能性表示食品。
健康に資する製品が手元に届きやすくなるという意味で、適切に運用されれば消費者にとっても企業にとってもメリットになりうる可能性を持つ制度です。
しかし今回、消費者庁の報告書などを読んだ印象としては、国の厳しい規制のもとで製造・販売される医薬品や、少なくとも申請の際には国による審査が行われる「特定保健食品(トクホ)」と比べて、残念ながら信頼をおける状況ではなさそうです。
少なくとも機能性表示食品については、機能性・安全性を国や公的機関が審査したものではなく、信じるどうかは「消費者の自己責任」ということだけでも覚えておく意味はありそうです。
執筆:市川衛ツイッターやってます。良かったらフォローくださいませ