新型コロナワクチンの「2回目難民」 2回目の接種が遅れても大丈夫か?
「2回目難民」
モデルナ社製のワクチンは4週間あけて合計2回、ファイザー社製のワクチンは3週間あけて合計2回(図)、接種する必要があります。

しかし、現在ワクチンの供給量が追い付いておらず、1回目を接種した後にもかかわらず、2回目の接種ができない「2回目難民」が増加しています。この場合、ワクチンの接種は遅れても大丈夫でしょうか?
1回のみの接種でもある程度効果はありますが、初回免疫だけでは変異ウイルスに対する効果が減弱することや効果に個人差が大きいことから、2回接種で効果をより高める必要があります。
ファイザー社製ワクチンは、「1回目の接種から3週間を超えた場合には、できる限り速やかに2回目の接種を実施すること」としていますので、基本的にはこれを守ってワクチン接種を受けることになります。
ではどのくらい空いても大丈夫なのでしょうか。
結論から書くと、6週間空いても問題ありません。また、最新のデータからは11~12週間くらい空いても大丈夫かもしれません。
2回目接種が遅れても十分な抗体が得られる
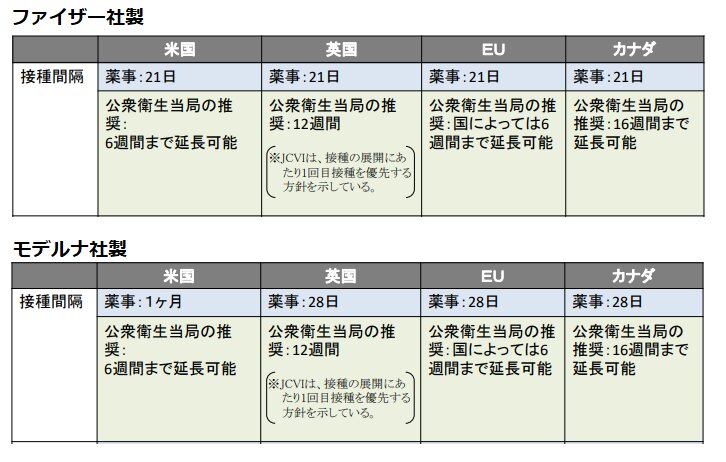
海外では、2回目のワクチン接種を遅らせて1回目のワクチン接種を大勢に行った方が、結果的に全体の死亡抑制効果が大きいという報告(1)を受けて、とにかく1回目の接種を優先しよう、としている国もあります。実際、流行がひどかったイギリスでは2回目の接種が12週間後などのように、かなり後ずれしています(表)。
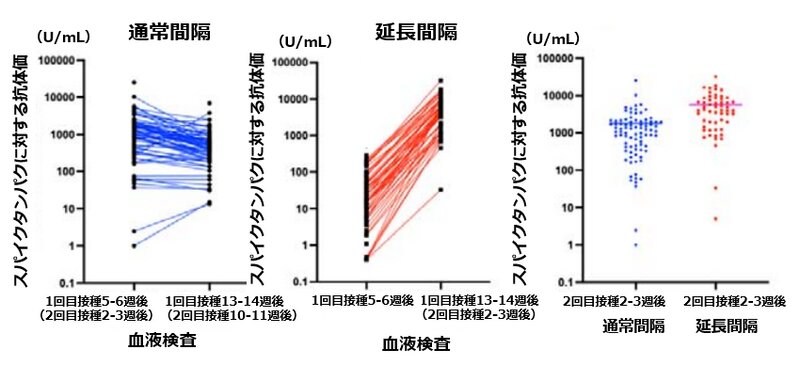
また、ファイザー社製ワクチンを規定通り3週空けて接種した群、あるいは11~12週間空けて接種した群に分けて比較した高齢者における抗体を推移をみたイギリスの研究があります(2)(査読前論文)。この抗体には、「新型コロナウイルスが入ってきたときに速やかに攻撃態勢を作る」という役割があります。
左のグラフが通常間隔(3週間)で接種した群、真ん中のグラフが延長間隔(11~12週間)で接種した群の抗体価の対数表示です。いずれも高い抗体価が得られています。延長間隔の場合、2回目でグンと抗体価が増えているのが分かります。驚くべきことに、11~12週間空けたほうがピーク抗体価の平均値が、約3.5倍高いという結果が得られました(右のグラフ)。
ただし、この研究では、「新型コロナウイルスに対する攻撃法をT細胞に覚えこませて、直接ウイルスを撃退する」という細胞性免疫の指標に関しては、間隔をあけた場合より弱いという結果でした。ただし、ワクチンによる細胞性免疫指標が新型コロナで重要なのかまだはっきりしていません。
ところで、アストラゼネカ社製の新型コロナワクチンは少し異なるメカニズムですが、これも接種間隔を延長した場合に、スパイクタンパクに対する抗体価が2.3倍に増加し、ワクチンによる感染予防効果が向上することが示されています(3)。
まとめ
現時点では、「2回目接種までのベストな間隔は規定通りの3週間で、公衆衛生当局としては6週間でも問題ないとしており、データからは11~12週間くらい間隔が空いても問題なさそうだ」ということが分かります。
ファイザー社製ワクチンのデータばかり紹介しましたが、モデルナ社製でも同様の考えになると思います。ただしアメリカ疾病予防管理センター(CDC)は、ファイザー社製もモデルナ社製も、いずれも6週間までしか保証できないと明言していますので(4)、基本的には推奨通り「原則上限6週間」と理解しておくべきでしょう※。
2回目接種までの間が空いてしまうと、「早く打たないと」とヤキモキすると思いますが、間隔が空いてもその後の感染予防効果は保証されるので、落ち着いて待つのがよいと思います。
1回の接種だけで終わると、その後新型コロナに感染するリスクは残ります。そのため、あまり遅くならないよう、受けられるタイミングでしっかり2回目の接種を受けておくことが重要です。
※2021年7月8日19時追記:ワクチン供給に懸念がある場合、WHOは12週間の間隔を容認しています(5,6)。
(参考)
(1) Romero-Brufau S, et al. BMJ. 2021 May 12;373:n1087.
(2) Parry H, et al. medRxiv preprint doi: https://doi.org/10.1101/2021.05.15.21257017
(3) Voysey M, et al. Lancet . 2021 Mar 6;397(10277):881-891.
(4) Interim Clinical Considerations for Use of COVID-19 Vaccines Currently Authorized in the United States (URL: https://www.cdc.gov/vaccines/covid-19/clinical-considerations/covid-19-vaccines-us.html)
(5) Interim recommendations for use of the Pfizer–BioNTech COVID-19 vaccine, BNT162b2, under Emergency Use Listing. (URL:https://www.who.int/publications/i/item/WHO-2019-nCoV-vaccines-SAGE_recommendation-BNT162b2-2021.1)
(6) Interim recommendations for use of the Moderna mRNA-1273 vaccine against COVID-19 (URL: https://www.who.int/publications/i/item/interim-recommendations-for-use-of-the-moderna-mrna-1273-vaccine-against-covid-19)










