症状、予防、経過と治療… 新型コロナウイルス感染症とは? 現時点で分かっていること(2021年5月)

流行から1年以上が経過し、新型コロナウイルス感染症について様々なことが分かってきました。
流行状況、症状、治療、予防など現時点で分かっていることについてまとめています(記事の内容は2021年5月29日時点での情報です)。
新型コロナウイルスとは?
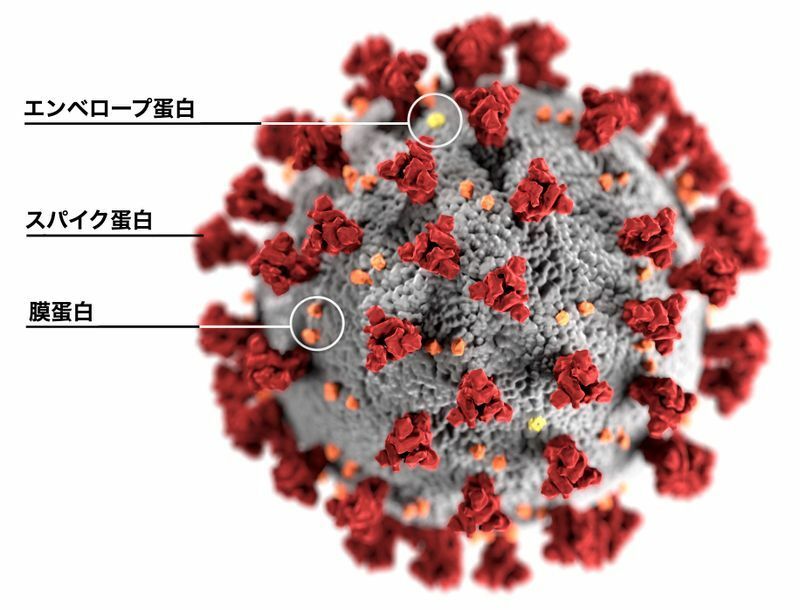
新型コロナウイルス(SARSコロナウイルス2)は、新型コロナウイルス感染症(COVID-19)の原因ウイルスで、RNAウイルスであるコロナウイルスの仲間です。
ウイルス粒子の表面にスパイク蛋白と呼ばれる突起があり、これが王冠のように見えることからコロナウイルスと名付けられました。
これまでにヒトに感染するコロナウイルスは4種類知られており、かぜの原因の10〜30%を占める原因ウイルスとして知られていました。
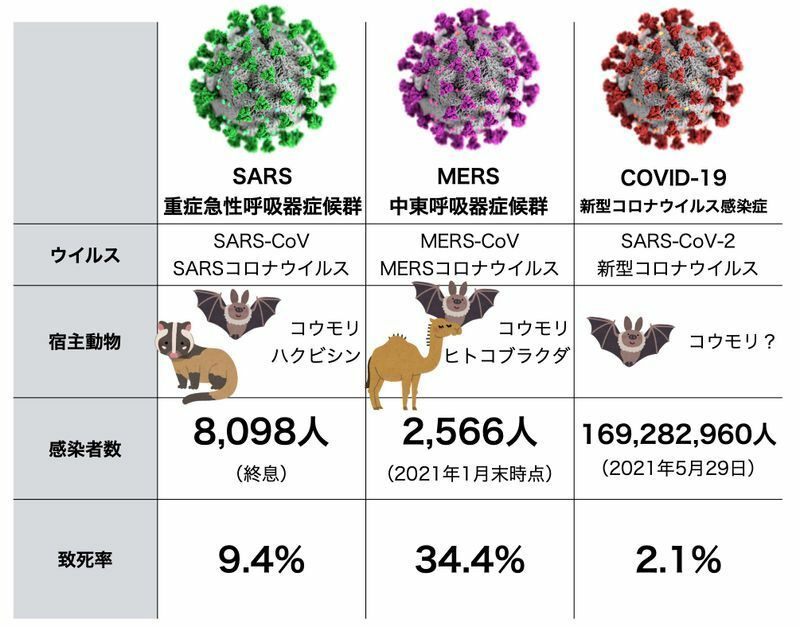
2002年中国広東省に端を発したSARS(重症急性呼吸器症候群)は、コウモリ(あるいはハクビシン)が持つコロナウイルスがヒトに感染し、ヒト-ヒト感染を起こすことで8000人を超える感染者を出しました。
また2012年には中東でMERS(中東呼吸器症候群)が報告され、ヒトコブラクダからヒトに感染する感染症であることが分かりました。
そして2019年12月末から中国の湖北省武漢市で発生した原因不明の肺炎は、新型のコロナウイルス(SARS-CoV-2)が原因であることが判明しました。
変異ウイルスとは?
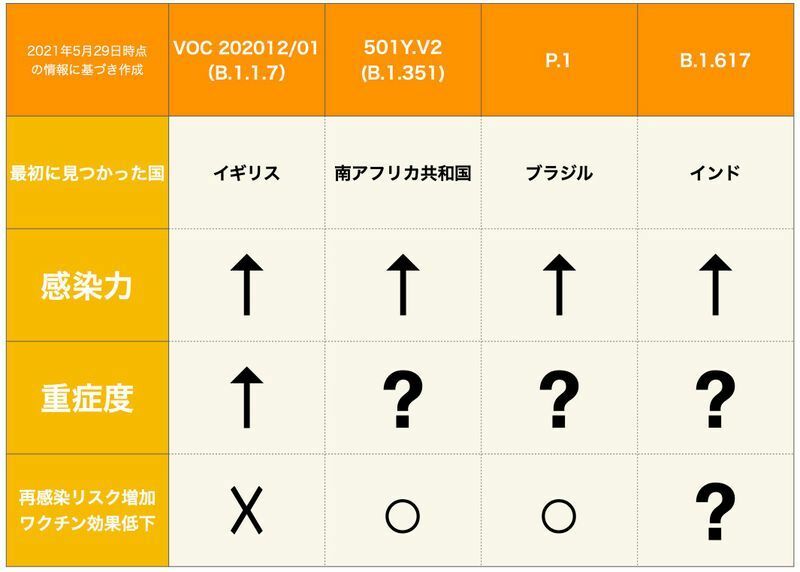
現在、世界中で変異ウイルスの拡大が問題になっています。
イギリスを起源とする変異ウイルス(B.1.1.7またはVOC 202012/01)はスパイク蛋白にN501Yという変異が起こることで感染力が強くなっています。また、従来のウイルスと比較して重症度も高くなることが分かっています。
南アフリカ共和国を起源とする変異ウイルス(B.1.351または501Y.V2)とブラジルを起源とする変異ウイルス(P.1)は、N501Yに加えてE484Kというスパイク蛋白の変異があり、感染力が強いだけでなく、過去の感染やワクチン接種によってできた免疫から逃れやすくなっていることから、再感染しやすくなったり、ワクチンの効果が低下することが懸念されています。
インドを起源とする変異ウイルス(B.1.617)は、まだ分かっていないことが多いものの、イギリス型と比べてさらに感染力が強い可能性が指摘されています。
新型コロナウイルスの世界での広がりは?
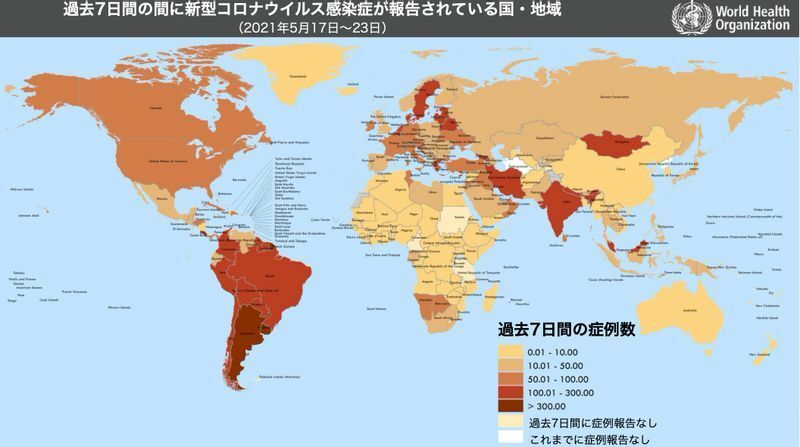
2021年5月29日時点での世界における新型コロナ患者は、
となっています。
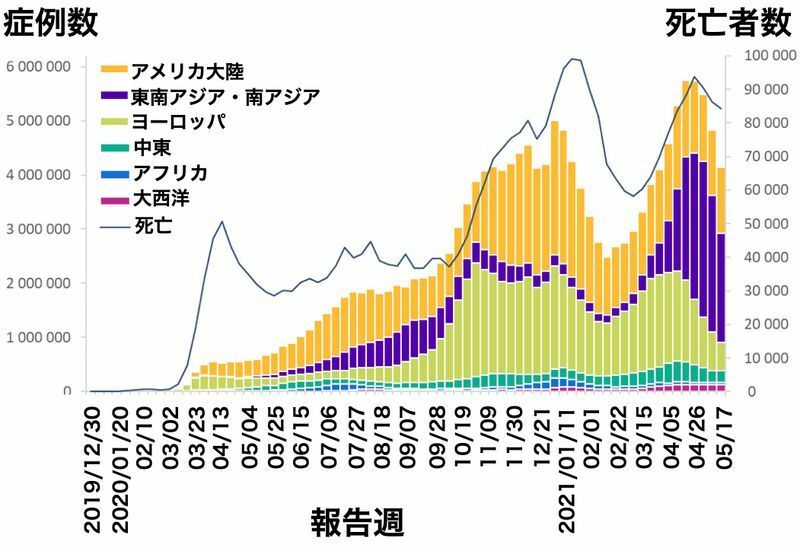
2019年12月から始まった流行は世界中に拡大し続け、欧米での感染者が大多数を占めていた2021年1月に一度流行のピークに達し減少傾向となりましたが、インドでの感染者増加に伴い2月下旬から再増加に転じ、4月下旬に二度目のピークを迎えました。
現在はインド、アメリカ、ブラジルで特に多くの感染者数が報告されています。
新型コロナウイルスの日本での広がりは?
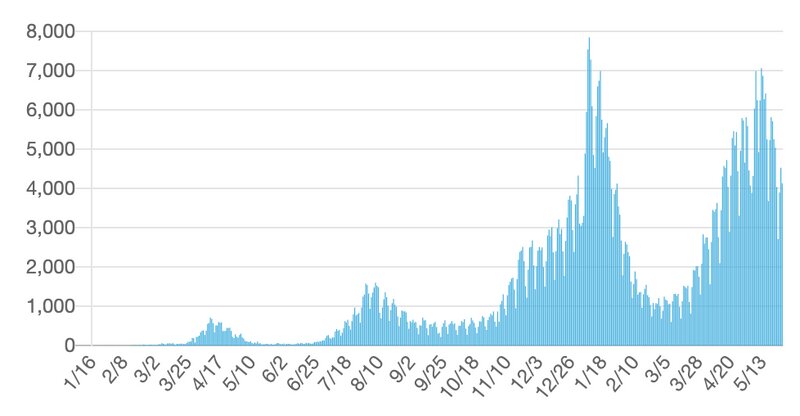
2021年5月29日時点での日本国内での新型コロナ感染者の報告数は、
となっています。
新型コロナウイルス感染症の症状は?

新型コロナの潜伏期間(感染する機会から何らかの症状を発症するまでの期間)には1〜14日と幅がありますが、多くの人がおよそ4〜5日で発症します。
新型コロナウイルス感染症の初期症状は風邪やインフルエンザと似ており、
・発熱
・咳
・だるさ
・食欲低下
・息切れ
・痰
・筋肉痛
・嗅覚障害・味覚障害
などの症状が見られることが多いです。
特に「息切れ」「嗅覚障害・味覚障害」の症状は、風邪やインフルエンザでは稀な症状ですので、新型コロナの可能性を疑うきっかけになります。
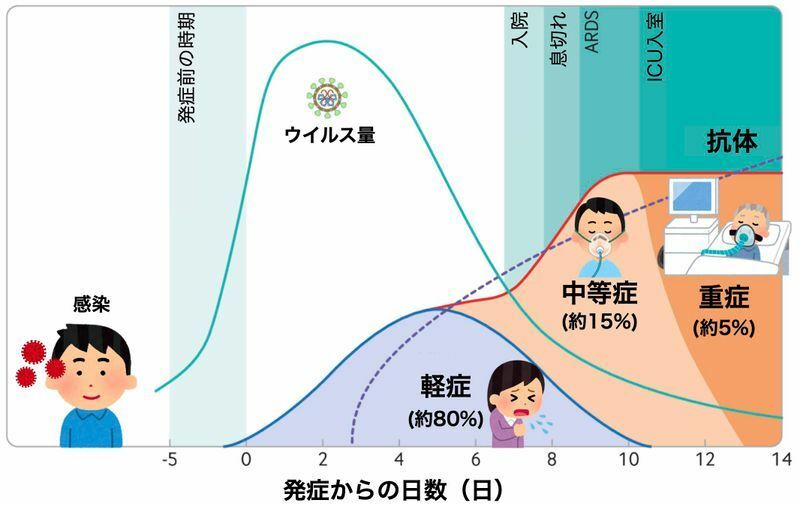
新型コロナに特徴的なのは、その経過です。
特に重症化する事例では、発症から1週間前後で肺炎の症状(咳・痰・呼吸困難など)が強くなってくることが分かっています。
流行早期の中国での4万人の感染者のデータによると、発症してから1週間程度は風邪のような軽微な症状が続き、約8割の方はそのまま治癒しますが、約2割弱と考えられる重症化する人は発症7日目前後から徐々に肺炎の症状が悪化して入院に至ります。
2割のうち全体の約5%の症例で発症から10日目前後に集中治療が必要になり、約2%の方が亡くなっています。
新型コロナウイルス感染症にかかると重症化しやすい人は?
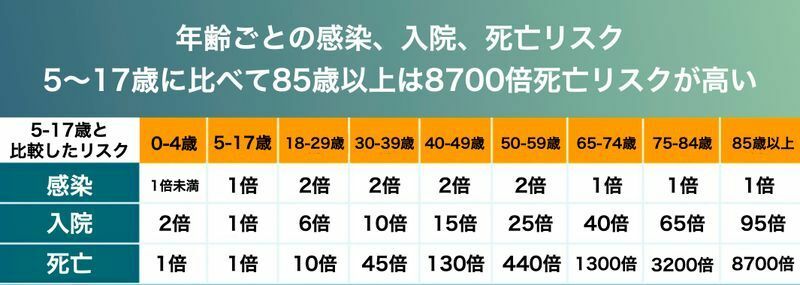
新型コロナウイルス感染症で重症化しやすいのは高齢者と持病のある方です。
アメリカのデータでは、5歳〜17歳を基準とした場合、85歳以上の死亡リスクは8700倍にもなります。
日本国内のデータからも年齢が上がれば上がるほど致死率が高くなることが示されています。
また、持病の有る無しによっても重症度が変わってくることも分かっています。
・65歳以上の高齢者
・男性
・悪性腫瘍
・慢性閉塞性肺疾患(COPD)
・慢性腎臓病
・2型糖尿病
・高血圧
・脂質異常症
・肥満 (BMI30以上)
・喫煙
・固形臓器移植後の免疫不全
・妊娠後期
という持病や嗜好、背景を持っている方は重症化しやすいことが知られています。
これらの基礎疾患や嗜好、背景は、複数あるほど入院リスクや死亡リスクが高くなることが知られています。
新型コロナの後遺症にはどんな症状がある?

新型コロナに感染した人のうちほとんどの人は回復後、通常の健康状態に戻る一方で、回復した後も数週〜数ヶ月間様々な症状が続く方がいます。
新型コロナ後遺症として頻度が高い症状には、
- 倦怠感:15~87%
- 息苦しさ:10~71%
- 胸の痛みや違和感:12~44%
- 咳:17~26%
などがあります。
これ以外にも、嗅覚障害、関節痛、頭痛、目や口の乾燥、鼻炎、味覚障害、食欲低下、めまい、筋肉痛、不眠症、脱毛、発汗、下痢、精神機能障害・認知機能障害などの症状が後遺症として報告されてます。
新型コロナウイルスの診断は?
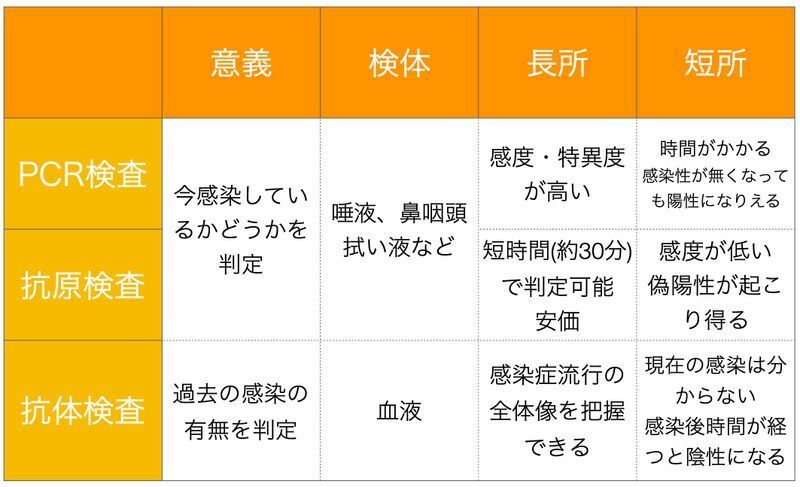
新型コロナウイルス感染症の確定診断には「PCR検査」または「抗原検査」が用いられています。
PCR検査とは、ウイルスの遺伝子を検出する検査です。
新型コロナウイルス感染症の患者ではノドの奥や痰の中、唾液などに新型コロナウイルスが存在するため、鼻咽頭を拭ったり唾液を採取したりして、その検体の中のウイルスの有無を検査します。
PCR検査はウイルスの遺伝子が少数であっても検出できるため、一般的に感染症の検査の中では検出力の高い検査とされます。
しかし、PCR検査で新型コロナ患者を100%診断できるわけではなく、感染者でも結果が陰性と出てしまうことがあります(偽陰性)。
また、周囲に感染をさせてしまう期間を過ぎてもPCR検査が陽性になり続けることがあります。
PCR検査以外に抗原検査も用いられるようになってきました。
抗原とはウイルスの一部であるタンパク質であり、抗原検査はこれを検出することで診断します。
抗原検査は30分という短時間で検査結果を得られる点、そしてPCR検査と異なり抗原検査は感染性のある期間だけ陽性になることが長所です。
一方で、抗原検査ではある程度のウイルス量がないと検出できないため抗原検査では陰性であってもPCR検査では陽性ということがありえます。
また抗原検査はPCR検査と比較して偽陽性(感染していないのに陽性と出てしまう)の事例が多く報告されています。
抗体検査は過去の感染を診断するための検査です。
抗体とは、生体の免疫反応によって体内で作られるものであり、微生物などの異物に攻撃する武器の一つです。
新型コロナウイルスでは発症から概ね2週間くらいで8割の人が、概ね3週間くらいでほぼ全ての人がIgMまたはIgGが陽性になります。
抗体検査は個人個人の診断というよりも、感染症の全体像を把握し、公衆衛生上の対策に役立てることができます。
ただし、特に無症候性感染者や軽症者では抗体が長期間維持されないという報告が出ており、過去に感染した人も抗体検査が陰性と出てしまうこともあります。
新型コロナウイルスの治療は?
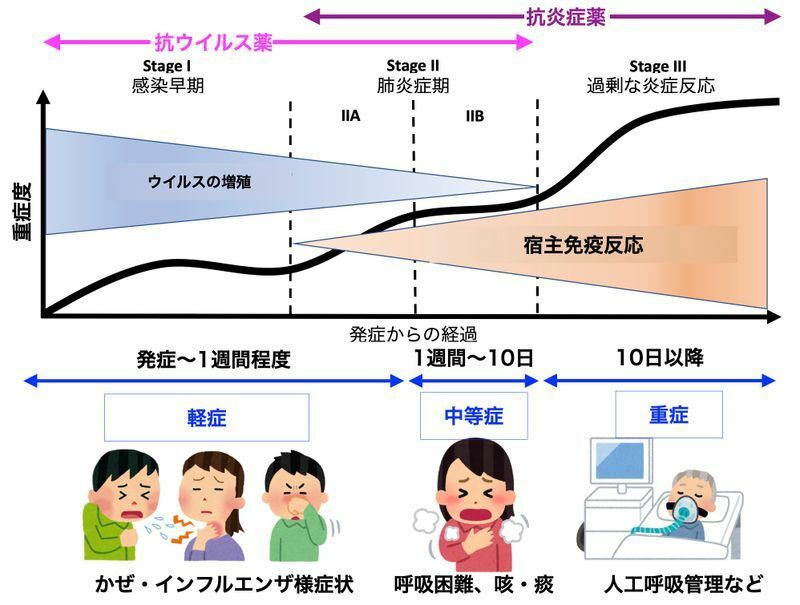
新型コロナウイルス感染症に対して有効性が確認されている薬剤が徐々に増えてきています。
発症初期のウイルス増殖期には抗ウイルス薬、そして発症から7〜10日以降の過剰な炎症反応が起こる時期には抗炎症薬を用いるという考え方が定着してきました。
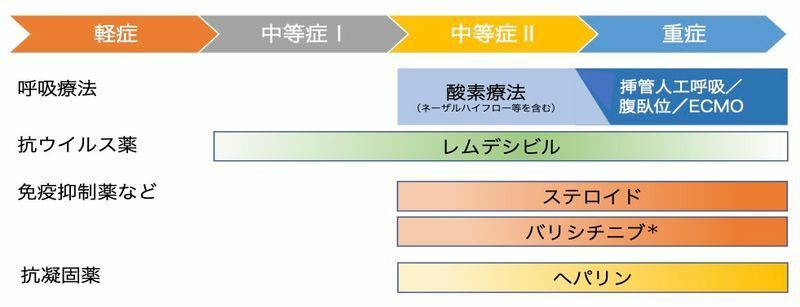
抗ウイルス薬としてはレムデシビル、抗炎症薬としてはデキサメタゾンおよびバリシチニブが国内では新型コロナに対して使用可能になっています。
これ以外にも、海外の臨床研究でトシリズマブの有効性も示されています。
さらに、新型コロナでは血が固まりやすくなる凝固異常が起こることが知られており、血をサラサラにする抗凝固薬としてヘパリンなどが用いられています。
新型コロナウイルス感染症の予防は?
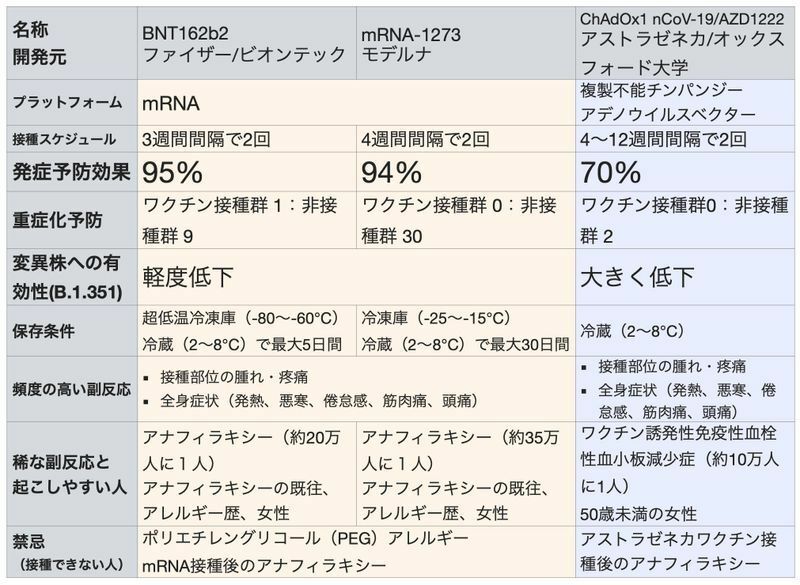
2021年5月29日時点で3つの新型コロナワクチンが国内で承認されています。
ファイザー社とモデルナ社のワクチンは同じmRNAワクチンというプラットフォームであり、接種間隔、保存条件、アナフィラキシーの頻度など多少の違いはありますが、効果や副反応においては概ね同等と考えられます。
どちらも発症予防効果90%以上と極めて高い「ぱねえ効果」を示しており、また重症化も防ぐことができます。
約20〜35万人に1人くらいの頻度でアナフィラキシーが起こることがあり、特に薬剤などにアレルギーのある方、アナフィラキシーの既往のある方で起こりやすいことが分かっています。いずれもmRNAワクチンの成分であるポリエチレングリコール(PEG)が原因と考えられており、PEGにアレルギーのある方は原則として接種できません。
アストラゼネカ社の新型コロナワクチンはウイルスベクターワクチンという技術を用いています。
同様に2回接種が必要であり、1回目から4〜12週空けて2回目を接種します。
発症予防効果は70.4%と報告されており、mRNAワクチンの90%以上と比べると見劣りするかもしれませんが、十分な効果があり、重症化を防ぐ効果も報告されています。
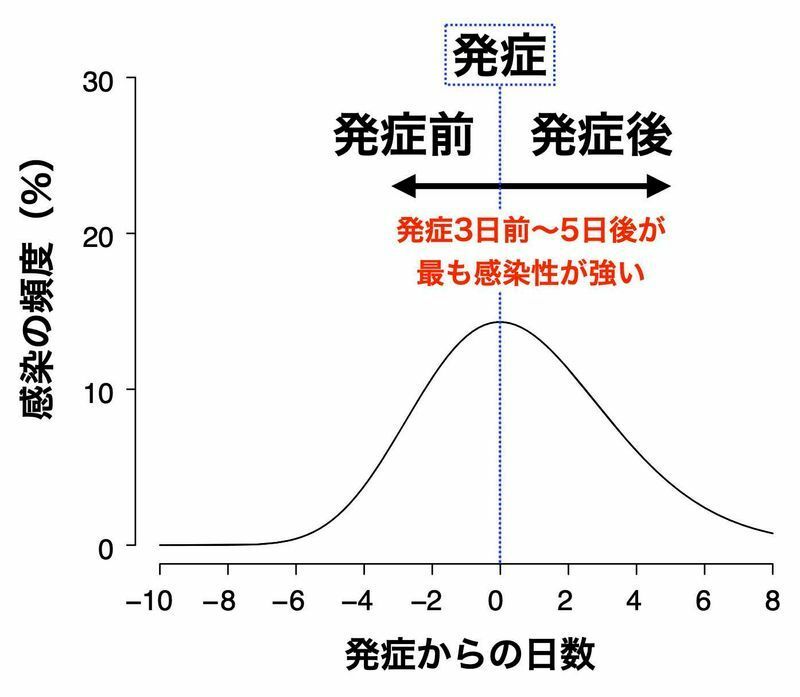
新型コロナはインフルエンザなどと違い、発症する前の状態から人にウイルスをうつすことがあります。
そのため、症状がない人も含めて屋内ではマスクを着用することが推奨されています。
新型コロナに感染した人が周囲の人にうつしやすい時期は、発症の3日前から発症後5日くらいであるとされます。この時期を過ぎると人にうつすことは稀になります。
新型コロナウイルス感染症は、「密閉・密集・密接」の3要素を持つ空間で広がりやすいことも分かっています。
老若男女、全ての人が「3密空間」を避けることが新型コロナ対策では重要です。
また手など触ったところからウイルスが広がり感染する可能性もあるため、こまめな手洗いを行うようにしましょう。

参考文献:
1.Isaacs D, Flowers D, Clarke JR, Valman HB, MacNaughton MR. Epidemiology of coronavirus respiratory infections. Archives of disease in childhood 1983; 58(7): 500-3.
2.Gaunt ER, Hardie A, Claas EC, Simmonds P, Templeton KE. Epidemiology and clinical presentations of the four human coronaviruses 229E, HKU1, NL63, and OC43 detected over 3 years using a novel multiplex real-time PCR method. Journal of clinical microbiology 2010; 48(8): 2940-7.
3.Monto AS. Medical reviews. Coronaviruses. The Yale journal of biology and medicine 1974; 47(4): 234-51.
4.Callow KA, Parry HF, Sergeant M, Tyrrell DA. The time course of the immune response to experimental coronavirus infection of man. Epidemiology and infection 1990; 105(2): 435-46.
5.Zhu N, Zhang D, Wang W, et al. A Novel Coronavirus from Patients with Pneumonia in China, 2019. The New England journal of medicine 2020; 382(8): 727-33.
6.Li Q, Guan X, Wu P, et al. Early Transmission Dynamics in Wuhan, China, of Novel Coronavirus-Infected Pneumonia. The New England journal of medicine 2020.
7.Guan WJ, Ni ZY, Hu Y, et al. Clinical Characteristics of Coronavirus Disease 2019 in China. The New England journal of medicine 2020.
8.Stokes EK, Zambrano LD, Anderson KN, et al. Coronavirus Disease 2019 Case Surveillance - United States, January 22-May 30, 2020. MMWR Morbidity and mortality weekly report 2020; 69(24): 759-65.
9.Cheung KS, Hung IFN, Chan PPY, et al. Gastrointestinal Manifestations of SARS-CoV-2 Infection and Virus Load in Fecal Samples From a Hong Kong Cohort: Systematic Review and Meta-analysis. Gastroenterology 2020; 159(1): 81-95.
10.Tong JY, Wong A, Zhu D, Fastenberg JH, Tham T. The Prevalence of Olfactory and Gustatory Dysfunction in COVID-19 Patients: A Systematic Review and Meta-analysis. Otolaryngol Head Neck Surg 2020; 163(1): 3-11.
11.Cevik M, Kuppalli K, Kindrachuk J, Peiris M. Virology, transmission, and pathogenesis of SARS-CoV-2. Bmj 2020; 371: m3862.
12.Huang C, Wang Y, Li X, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet (London, England) 2020; 395(10223): 497-506.
13.Matsunaga N, Hayakawa K, Terada M, et al. Clinical epidemiology of hospitalized patients with COVID-19 in Japan: Report of the COVID-19 REGISTRY JAPAN. Clinical infectious diseases : an official publication of the Infectious Diseases Society of America 2020.
14.Liang W, Guan W, Chen R, et al. Cancer patients in SARS-CoV-2 infection: a nationwide analysis in China. The Lancet Oncology 2020; 21(3): 335-7.
15.Lippi G, Henry BM. Chronic obstructive pulmonary disease is associated with severe coronavirus disease 2019 (COVID-19). Respir Med 2020; 167: 105941.
16.Myers LC, Parodi SM, Escobar GJ, Liu VX. Characteristics of Hospitalized Adults With COVID-19 in an Integrated Health Care System in California. Jama 2020; 323(21): 2195-8.
17.Fadini GP, Morieri ML, Longato E, Avogaro A. Prevalence and impact of diabetes among people infected with SARS-CoV-2. J Endocrinol Invest 2020; 43(6): 867-9.
18.Zheng Z, Peng F, Xu B, et al. Risk factors of critical & mortal COVID-19 cases: A systematic literature review and meta-analysis. J Infect 2020; 81(2): e16-e25.
19.Yang J, Zheng Y, Gou X, et al. Prevalence of comorbidities and its effects in patients infected with SARS-CoV-2: a systematic review and meta-analysis. International journal of infectious diseases : IJID : official publication of the International Society for Infectious Diseases 2020; 94: 91-5.
20.Popkin BM, Du S, Green WD, et al. Individuals with obesity and COVID-19: A global perspective on the epidemiology and biological relationships. Obes Rev 2020; 21(11): e13128.
21.Latif F, Farr MA, Clerkin KJ, et al. Characteristics and Outcomes of Recipients of Heart Transplant With Coronavirus Disease 2019. JAMA Cardiol 2020.
22.Mahdavinia M, Foster KJ, Jauregui E, et al. Asthma prolongs intubation in COVID-19. J Allergy Clin Immunol Pract 2020; 8(7): 2388-91.
23.Brenner EJ, Ungaro RC, Gearry RB, et al. Corticosteroids, But Not TNF Antagonists, Are Associated With Adverse COVID-19 Outcomes in Patients With Inflammatory Bowel Diseases: Results From an International Registry. Gastroenterology 2020; 159(2): 481-91.e3.
24.Michelena X, Borrell H, López-Corbeto M, et al. Incidence of COVID-19 in a cohort of adult and paediatric patients with rheumatic diseases treated with targeted biologic and synthetic disease-modifying anti-rheumatic drugs. Semin Arthritis Rheum 2020; 50(4): 564-70.
25.Hadi YB, Naqvi SFZ, Kupec JT, Sarwari AR. Characteristics and outcomes of COVID-19 in patients with HIV: a multicentre research network study. Aids 2020; 34(13): F3-f8.
26.Ellington S, Strid P, Tong VT, et al. Characteristics of Women of Reproductive Age with Laboratory-Confirmed SARS-CoV-2 Infection by Pregnancy Status - United States, January 22-June 7, 2020. MMWR Morbidity and mortality weekly report 2020; 69(25): 769-75.
27.Allotey J, Stallings E, Bonet M, et al. Clinical manifestations, risk factors, and maternal and perinatal outcomes of coronavirus disease 2019 in pregnancy: living systematic review and meta-analysis. Bmj 2020; 370: m3320.
28.COVID-19レジストリデータを用いた新型コロナウイルス感染症における年齢別症例致命割合について.
29.Carfì A, Bernabei R, Landi F. Persistent Symptoms in Patients After Acute COVID-19. Jama 2020; 324(6): 603-5.
30.Garrigues E, Janvier P, Kherabi Y, et al. Post-discharge persistent symptoms and health-related quality of life after hospitalization for COVID-19. J Infect 2020.
31.Miyazato Y, Morioka S, Tsuzuki S, et al. Prolonged and late-onset symptoms of coronavirus disease 2019. Open Forum Infectious Diseases 2020.
32.Shi H, Han X, Jiang N, et al. Radiological findings from 81 patients with COVID-19 pneumonia in Wuhan, China: a descriptive study. The Lancet Infectious diseases 2020.
33.Wang W, Xu Y, Gao R, et al. Detection of SARS-CoV-2 in Different Types of Clinical Specimens. Jama 2020; 323(18): 1843-4.
34.Williams E, Bond K, Zhang B, Putland M, Williamson DA. Saliva as a Noninvasive Specimen for Detection of SARS-CoV-2. Journal of clinical microbiology 2020; 58(8).
35.Wyllie AL, Fournier J, Casanovas-Massana A, et al. Saliva or Nasopharyngeal Swab Specimens for Detection of SARS-CoV-2. The New England journal of medicine 2020; 383(13): 1283-6.
36.Organization WH. Laboratory biosafety guidance related to coronavirus disease 2019 (COVID-19): interim guidance, 12 February 2020: World Health Organization, 2020.
37.Ogawa T, Fukumori T, Nishihara Y, et al. Another false-positive problem for a SARS-CoV-2 antigen test in Japan. J Clin Virol 2020; 131: 104612.
38.Gandhi RT, Lynch JB, Del Rio C. Mild or Moderate Covid-19. The New England journal of medicine 2020; 383(18): 1757-66.
39.Wang M, Cao R, Zhang L, et al. Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro. Cell research 2020; 30(3): 269-71.
40.Wang Y, Zhang D, Du G, et al. Remdesivir in adults with severe COVID-19: a randomised, double-blind, placebo-controlled, multicentre trial. Lancet (London, England) 2020; 395(10236): 1569-78.
41.Beigel JH, Tomashek KM, Dodd LE, et al. Remdesivir for the Treatment of Covid-19 - Preliminary Report. The New England journal of medicine 2020.
42.Goldman JD, Lye DC, Hui DS, et al. Remdesivir for 5 or 10 days in patients with severe Covid-19. New England Journal of Medicine 2020.
43.Spinner CD, Gottlieb RL, Criner GJ, et al. Effect of Remdesivir vs Standard Care on Clinical Status at 11 Days in Patients With Moderate COVID-19: A Randomized Clinical Trial. Jama 2020.
44.Repurposed Antiviral Drugs for Covid-19 — Interim WHO Solidarity Trial Results. New England Journal of Medicine 2020.
45.Grein J, Ohmagari N, Shin D, et al. Compassionate Use of Remdesivir for Patients with Severe Covid-19. The New England journal of medicine 2020.
46.Horby P, Lim WS, Emberson JR, et al. Dexamethasone in Hospitalized Patients with Covid-19 - Preliminary Report. The New England journal of medicine 2020.
47.Wang D, Hu B, Hu C, et al. Clinical Characteristics of 138 Hospitalized Patients With 2019 Novel Coronavirus-Infected Pneumonia in Wuhan, China. Jama 2020.
48.Cheng PK, Wong DA, Tong LK, et al. Viral shedding patterns of coronavirus in patients with probable severe acute respiratory syndrome. Lancet (London, England) 2004; 363(9422): 1699-700.
49.Oboho IK, Tomczyk SM, Al-Asmari AM, et al. 2014 MERS-CoV outbreak in Jeddah--a link to health care facilities. The New England journal of medicine 2015; 372(9): 846-54.
50.Klompas M, Morris CA, Shenoy ES. Universal Masking in the Covid-19 Era. The New England journal of medicine 2020; 383(2): e9.
51.Wang X, Ferro EG, Zhou G, Hashimoto D, Bhatt DL. Association Between Universal Masking in a Health Care System and SARS-CoV-2 Positivity Among Health Care Workers. Jama 2020.
52.Brooks JT, Butler JC, Redfield RR. Universal Masking to Prevent SARS-CoV-2 Transmission—The Time Is Now. Jama 2020.
53.Polack FP, Thomas SJ, Kitchin N, et al. Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine. New England Journal of Medicine 2020; 383(27): 2603-15.